
[헬스코리아뉴스 / 이시우] 브이티의 계열사인 브이티바이오는 현재 국내 임상 1상을 완료한 VT301(항원 특이적 조절 T세포)이 대표적 치매 동물 모델인 5xFAD 마우스 모델에서 베타 아밀로이드 농도 및 타우인산화를 획기적으로 낮추며, 각종 염증 지표가 개선된다는 결과를 확인했다고 12일 주장했다.
회사측에 따르면 이전 Theranostics 2022; 12(18):7668-7680에 게재된 논문에서는 치매의 또 다른 대표적 동물모델인 3xTg 마우스 모델에서 VT301의 효능을 확인했다. 현재 VT301은 미국 FDA에서 임상 1/2a를 허가 받아 이에 대한 준비 과정 중에 있다.
면역세포의 일종인 조절 T세포(Regulatory T cell, Treg)는 면역억제를 유도하는 세포로 주로 자가면역 질환 등에 활용되는 세포치료제로 많은 연구가 진행되고 있다. 최근에는 중추신경계의 면역 균형을 유지시키는 역할도 밝혀지면서, 퇴행성 뇌질환에서 조절 T세포를 이용한 치료제 개발 기능성으로 발전 하고 있다.
브이티바이오와 경희대 연구팀은 퇴행성 뇌질환에 대한 조절 T세포 치료법을 연구한 결과 충분한 가능성을 실험을 통해 확인 하였고 문제가 있는 뇌에 세포를 보내기 위해 아밀로이드 베타를 항원으로 활용해 항원 특이적 조절 T세포를 배양하는 방법을 개발하여 GMP 시설에 공정세팅을 완료했다.
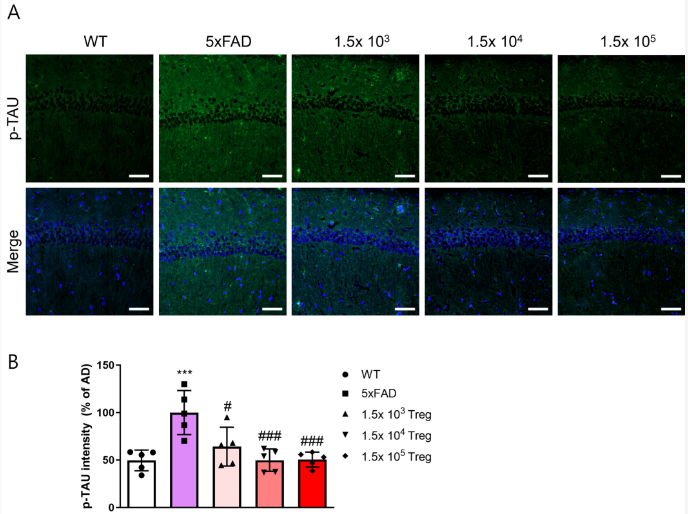
이러한 배양 기술을 기반으로 알츠하이머성 치매 동물 모델인 5xFAD에 투여하여 기억력 관련 행동실험인 Y미로 실험과 수동회피실험(PAT)을 진행하여 정상적인 쥐와 비슷한 학습 및 기억력 개선이 이루어 졌음을 확인했다. 또한 임상시험 시 대표적인 치매 바이오 마커인 베타 아밀로이드(Beta-amyloid)와 인산화 타우(p-Tau)의 축적이 정상 동물모델 정도까지 개선됨을 확인했다.
나아가 뇌 해마의 CA1 부위에서 염증 지표인 산화질소합성 효소(NOS2)가 50% 이하로 낮추어 졌다. 이외 염증 관련 지표인 TNF-a ,Arg-1 IL-1B 등도 모두 일관되게 줄어드는 현상을 관찰했다.
회사 관계자는 “이는 항원 특이적 조절 T세포인 VT301이 기존 조절 T세포에 비해 뇌로 이동하는 세포 수가 월등히 높고 뇌에 존재하는 미세아교세포의 활성화가 현저히 억제 되었기에 염증 관련 지표 모두가 개선되는 것으로 판단하고 있다”며, “이에 대한 논문은 International Journal of Molecular Science 저널에 Neurodegenerative Disease: From Molecular Basis to Therapy, 2nd Edition에 게재되었다”고 말했다.

브이티바이오는 “임상 1상 시험에서 도출된 결과를 현재 학술지 상위 25%에 있는 Q1급 퇴행성 뇌질환 분야 전문 국제 학술지에 제출하여 추가적으로 심사 중에 있다”며, “조만간 좋은 결과가 있을 것으로 예상하고 있다”고 주장했다.
회사측은 이어 “국내 임상시험으로 VT301의 세포 주입량 및 그 시기를 예측 할 수 있게 되어 일본의 세포체료제 전문 병원과 비밀유지계약을 완료하고 일본에서 VT301 배양을 진행하여 세포 동등성 테스트를 진행하고 있다”며, “관련 허가는 금년 상반기에 신청 후 빠르게 승인 작업을 진행하여 노년층이 많은 일본에서 서비스를 수행할 계획”이라고 강조했다.
그러면서 “최근 한국에서도 첨단재생의료 및 첨단바이오의약품법(첨생법)의 개정안이 관련 소위를 통과하여 한국에서의 서비스 실시가 기대되고 있다”며, “기존 미국에서의 임상시험은 허가 완료된 사항이라 관련 임상시험 대행기관(CRO)과 면밀한 협의를 통해 임상시험을 준비 중”이라고 설명했다.






