[헬스코리아뉴스 / 이순호 기자] 지난해 제네릭의약품 허가를 위해 승인받은 생물학적동등성계획 승인건수가 106건으로 전년(123건) 대비 약 13.8% 감소한 것으로 나타났다.
식품의약품안전처는 21일 이같은 내용의 제네릭의약품 개발동향 분석 결과를 발표하고 “2011년 이후 여러 제약사가 공동으로 생동성시험을 진행하거나 수익성이 높은 제품의 공동개발 등으로 지속적으로 감소 추세에 있으며, 특히 지난해 승인건수 감소는 2018년 만료되는 재심사 및 특허 대상 품목이 감소한데 따른 것으로 분석된다”고 설명했다.
지난해 승인된 생동성시험의 주요 특징은 ▲재심사·특허만료 의약품 개발 집중 ▲치료영역별로 대사성의약품, 중추신경계용의약품, 순환계의약품 개발 추세 지속 등이다.
지난해 승인된 생동계획서 중 재심사나 특허 만료 예정 품목에 대한 비중은 56건(53%)으로 절반을 차지했다. 이 가운데 생산실적이 높고 지난해 11월 재심사가 만료된 당뇨병성 다발성 신경염 치료제 ‘알티옥트산트로메타민염’ 제품(13건) 개발이 가장 많았다.
이어 당뇨병치료제 리나글립틴·메트포르민염산염(5건), 고혈압치료제 암로디핀베실산염·올메사르탄메독소밀·히드로클로로티아지드(5건) 개발이 많았다.
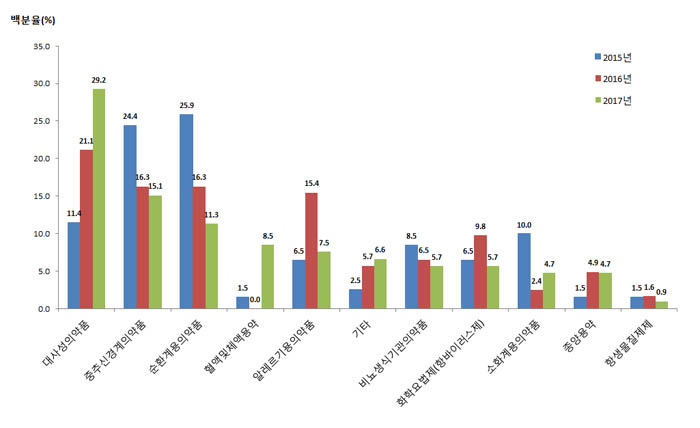

치료영역별로는 노인 인구 증가로 인한 당뇨병치료제 등 대사성의약품(31건, 29.2%), 치매 등에 사용하는 중추신경계용의약품(16건, 15.1%), 고혈압치료제 등 순환계용의약품(12건, 11.3%) 순으로 개발이 활발하게 이루어지는 것으로 나타났다.
대사성, 순환계, 중추신경계의약품 개발은 매년 꾸준히 이루어지고 있으며, 전체 승인건수의 절반 이상(55.6%)을 차지했다.
식약처 관계자는 “대사성의약품 승인건수가 가장 많은 것은 당뇨병성 다발성 신경염 치료제 ‘알티옥트산트로메타민염’(13건) 개발이 증가하고, 2016년에 이어 당뇨병치료제 ‘리나글립틴’(6건, 복합제 포함) 개발이 지속적으로 이루어진데 따른 것”이라고 설명했다.






