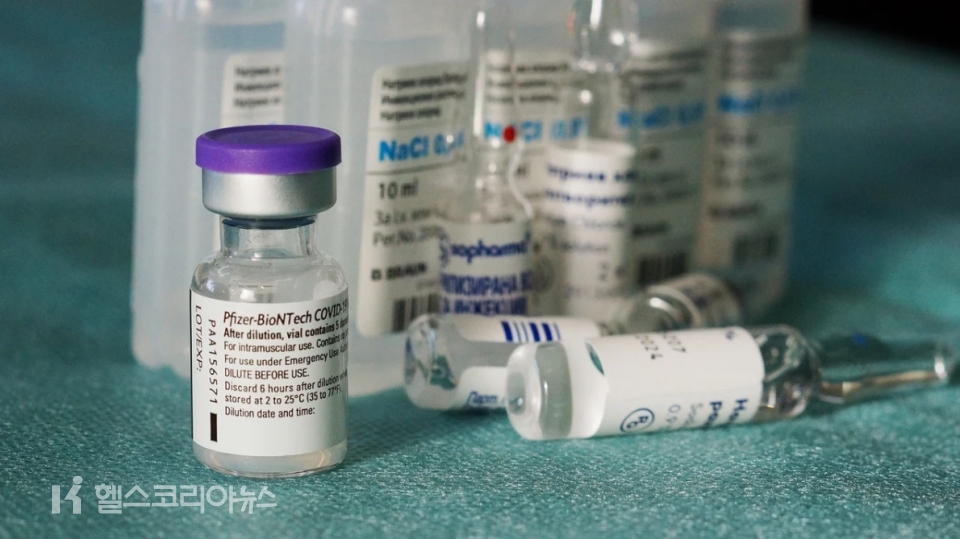
[ソウル/ヘルスコリアニュース] 保健当局が5日、ファイザーのコロナ19ワクチン「コミナティージュ」(Comirnaty Inj. 成分名:トニー·ナメラン·Tozinameran)の国内販売を許可した。 アストラゼネカの「韓国アストラゼネカコビド-19ワクチン酒」(AstraZeneca Korea Covid-19 Vaccine Inj.)に続き国内で許可を受けた2番目のコロナ19ワクチンである。
食品医薬品安全処はこの日、コロナ19ワクチン最終点検委員会会議を開き、「コミナティ州」の臨床試験最終結果報告書などを許可後に提出する条件で市販を承認したと明らかにした。
「コミナティ州」は米国ファイザーとドイツのバイオエンテックが共同開発したmRNAワクチンだ。 コロナ19ウイルス抗原遺伝子をmRNAの形で注入して体内で抗原タンパク質を合成し、このタンパク質が中和抗体の生成を誘導してコロナ19ウイルスが人体に侵入した時、ウイルスを中和して除去する。
16歳以上で投薬が可能で、希釈後0.3ミリリットルを1回接種した後、3週間後に追加接種する。 保管条件は零下60~90℃から6カ月である。 物理的な力によって構造が分解しやすいため「柔らかくひっくり返す」「揺らがない」を使用上の注意事項に含めるようにした。
「コミナティ州」はmRNAワクチンとしては国内で初めて許可されるワクチンだ。 この他にも欧州(EMA)、米国、日本など59カ国で、そしてWHOから条件付きの許可または緊急使用承認を受けている。

食薬処は、「安全を最優先に、科学的根拠に基づいて今回の品目許可を決めた」と説明した。
ワクチンの安全性については、報告された異常事例の大半が、軽症から中間レベルであり、ワクチン接種後数日内に回復するという。 薬物関連の過敏反応(蕁麻疹)は1件発生し、急激な全身反応を意味する「アナフィラキシー」反応は臨床試験期間中に報告されなかった。
臨床試験登録対象者4万3448人のうちワクチン群0.6%(126人)、対照群0.5%(111人)で「重大な異常事例」が報告され、このうちワクチン投与との関連性を排除できない「重大な薬物異常反応」は肩部の傷など4件だった。
有効性に関しては、米国等で実施した多国家臨床試験においてコロナ19 陰性の16 歳以上3 万6523 人を評価した結果が根拠とされた。
臨床試験被験者のうちコロナ19の確定判定を受けた人はワクチン群8人、対照群162人で、「コミナティ州」は約95%の予防効果を見せた。
食薬処は16歳以上を対象に品目を許可した背景について「臨床試験が16歳以上の対象者で安全性と効果性を確認するように設計されて予防効果が確認された点、16歳以上の青少年の免疫反応が成人と変わらないと判断される点などを考慮した」と明らかにした。
米国、欧州、英国、日本など多数の国で「コミナティ株」の投薬対象年齢を16歳以上と許可した点を一緒に考慮したという説明だ。
食薬処は「コミナティ州」許可後、疾病庁などと協力して接種後の異常事例の監視をさらに強化する方針だ。






