[헬스코리아뉴스 / 박민주] 국내 의약품 제조사의 '마이크로니들 의약품'의 제품화 지원을 위해 정부가 구체적 가이드라인을 제정하며 지원에 나선다.
식품의약품안전처(처장 김강립)는 첨단 기술을 적용한 ‘마이크로니들 의약품’의 제품화 지원을 위해 규격설정 및 품질자료 작성 등 품질평가 기준 설정을 위한 가이드라인(민원인 안내서)을 25일 제정했다.
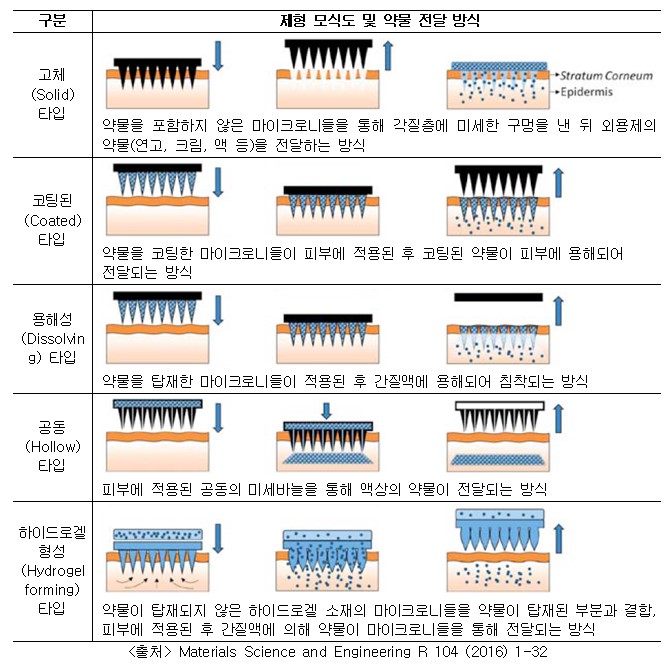
가이드라인의 주요 내용은 ▲마이크로니들 타입별 분류 ▲품질 규격 설정 시 고려사항 ▲특성이나 기능 등을 설정하기 위한 제제학적 시험 항목 등이다.
마이크로니들 의약품이란 미세한 바늘을 이용해 주성분을 혈관이 아닌 피부로 전달하는 방식의 의약품을 말한다. 통증이 매우 적어 투약 순응도가 높고, 감염 사고를 예방할 수 있는 등의 장점이 있어 기존 주사제나 경구용 제제의 단점을 극복할 수 있는 제형으로 주목받고 있다.
식약처에 따르면, 마이크로니들 의약품의 전 세계 시장 규모(퓨처마켓인사이트 리포트 2020)는 2015년 4억 7000만 달러(5279억 원)에서 2019년에는 6억 2160만 달러(6916억 원)로 확대됐다. 오는 2030년에는 12억 390만 달러(1조 3521억 원)에 이를 것으로 전망되고 있다.
식약처는 "이번 가이드라인이 국내 제약업체나 벤처기업의 임상시험 진입 등 마이크로니들 의약품 제품화에 도움을 줄 것으로 기대한다"고 말했다.






