[헬스코리아뉴스 / 이순호] 의약품 품질 관리 수준을 획기적으로 높일 수 있지만, 전문가가 없고 비용이 많이 드는 탓에 제약업계에 큰 부담을 안겼던 QbD(Quality by Design, 설계기반품질고도화)의 제도화가 시작됐다. 그동안 QbD를 알리는 데 집중해 온 정부는 제약사들이 QbD를 실무에 적용하도록 다양한 신호를 보내고 있어 QbD 시대 개막이 머지않았다는 관측이 나온다.
지난 1일 홍남기 부총리 겸 기획재정부 장관 주재로 개최한 제4차 혁신성장 BIG3 추진회의도 그 중 하나다. 정부는 이날 '바이오 생산경쟁력 확충 방안'을 확정했다. 이 방안에는 QbD를 이용한 생산 공정 모델을 개발하고 스마트 공장 보급을 확산해 QbD를 접목하는 내용이 포함됐다.
QbD는 사전 위험평가를 통해 의약품 개발부터 투약까지 모든 과정을 실시간으로 제품 특성에 맞게 최적의 품질로 관리하는 시스템이다. 정부가 이번 '바이오 생산경쟁력 확충 방안'을 통해 집중하려는 QbD 분야는 생산 단계 품질 관리 부문이다. QbD를 의약품 제조 시설에 적용해 품질경쟁력을 높이고 선진국과 기술격차를 줄이는 것이 목표다.
2022년부터 연속공정 도입 등 기술개발 추진
우선 정부는 혁신 제조기술 개발을 위해 오는 2022년부터 불량률 최소화, 연속공정 도입 등을 목표로 기술개발 사업을 추진한다는 방침이다. QbD 방식을 적용한 생산 공정 모델을 개발해 제품 품질을 고도화하고, 공정분석기술(PAT) 도입 등 QbD 기반의 연속공정 시스템 개발로 제조시간 단축과 함께 제조 비용 절감 기반을 마련할 계획이다.
이는 스마트공장 확충을 통해 진행할 예정인데, 정부는 중소·중견기업을 대상으로 첨단 정보통신기술과 접목한 제약 분야 스마트공장 구축을 지원하고, 스마트공장과 QbD 도입·확산 정책을 연계할 방침이다.
정부의 QbD 도입 정책은 이미 시작됐다. 식품의약품안전처는 QbD를 처음으로 제도권으로 끌어들이며 제약업계에 QbD 시대 도래를 알렸다.
식약처는 지난해 12월 17일 '의약품의 품목허가·신고·심사 규정' 개정 고시안을 행정예고하고, 의약품 품질 보증과 연관성이 증명된 디자인 스페이스(Design Space)를 제조 및 품질관리에 적용하는 의약품의 경우, 해당 디자인 스페이스 내용을 허가(신고)신청서 중 해당하는 부분에 기재할 수 있는 근거를 마련했다.
식약처, QbD 적용 제도적 근거 마련
QbD는 의약품 제조 공정에 대한 리스크 분석을 통해 핵심 공정을 결정하고 그 공정 운영 범위를 설정하도록 하는데, 여기에서 공정 운영 범위가 바로 디자인 스페이스다. 즉, 식약처는 QbD를 적용해 품질을 관리하는 의약품의 경우, 허가 신청서에 그 내용을 기재할 수 있도록 물꼬를 터 준 것이다.
QbD에 따른 디자인 스페이스를 설정하려면 진행해야 하는 실험의 수가 기하급수적으로 증가한다. 그만큼 제약사의 부담도 커진다. 그러나, 디자인스페이스 설정에 성공해 허가 신청서에 이를 기재하고 품목허가를 획득하면, 차후 제품 공정 과정의 일정 범위 내 변경을 제약사가 직접 할 수 있게 된다. 검증된 디자인 스페이스 안에서 공정을 변경하는 것은 제약사의 자율 관리 아래 가능해진다는 것이다.
다만, 이를 의무적으로 해야 하는 것은 아니다. 식약처 관계자는 본지와 통화에서 "QbD를 적용할 수 있도록 처음으로 제도적 근거를 마련한 것으로 의무화하려는 것은 아니다"라고 말했다.
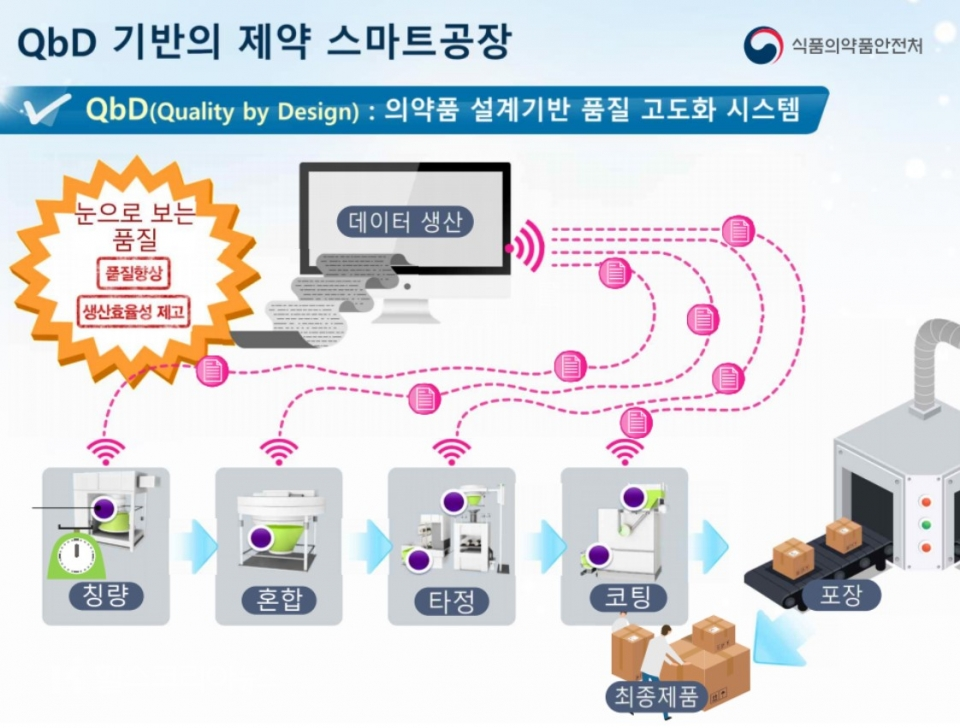
식약처의 QbD 제도화는 아직 초기 단계다. PAT(Process Analytical Technology, 공정 분석 기술)를 이용한 실시간 품질 모니터링, 과학적 제품 및 공정 설계를 위한 리스크 분석 (Risk Assessment) 및 실험계획법(DoE, Design of Experiments) 등 앞으로 추가해야 할 내용이 산더미다.
이 때문에 업계에서는 QbD가 의무화되기까지는 상당한 시간이 걸릴 것이라는 안심 섞인 전망이 나온다. 그러나, 연이어 의약품 품질 기준을 강화하고 있는 정부의 행보를 고려할 때, QbD 의무화도 시간문제라는 시각도 적지 않다.
“QbD는 강력한 품질 기준” ... “의무화 시간문제”
한 제약사 관계자는 "QbD는 리스크 분석, PAT, DoE, 디자인 스페이스 등 다양한 부문을 총망라하는 총체적 내용이지만, 이들 각 부문은 그 자체만으로도 하나의 강력한 품질 기준이 될 수 있다"며 "QbD를 전체로 한 번에 의무화한다기보다는 QbD의 세부 내용을 하나씩 의무화하는 방식으로 QbD를 제도에 녹여낼 가능성이 있다"고 말했다.
정부로부터 QbD 컨설팅을 받은 제약사들이 QbD 적용 후 눈에 보이는 성과를 내고 있는 점도 정책 추진에 힘을 실어주고 있다는 분석이다.
다른 제약사 관계자는 "최근 대웅제약의 QbD 적용 성과 발표가 있었다. 식약처의 컨설팅 사업을 통해 획기적인 효율 개선을 이뤘다고 한다"며 "이번 발표를 통해 식약처는 간접적으로 QbD 정책 홍보 효과를 누리게 됐다. 사실상 QbD 제도화에 더 힘이 실리고 속도가 붙지 않겠느냐"고 말했다.
대웅제약, QbD 성과 발표 ... 의약품 생산 효율화 기여
대웅제약은 지난달 21일 자사가 개발 중인 위식도역류질환 치료제 '펙수프라잔 주사제'의 QbD 컨설팅 프로젝트 성과를 발표했다. 이번 프로젝트는 대웅제약이 식약처가 주관하는 '맞춤형 QbD 전문 컨설팅사업'에 선정돼 지난해 8월부터 약 3개월간 진행했다. 박영준 아주대학교 교수와 김주은 대구가톨릭대학교 교수가 이끄는 연구팀의 QbD 컨설팅을 받아 제제설계부터 제조공정 개발, 공정분석기술, 생산규모 확대에 이르는 기술지원을 받았다.
그 결과, '펙수프라잔' 주사제의 동결건조 공정 시간은 절반으로 줄었고 생산비용은 35% 절감할 수 있게 됐다. 생산 가능 용량 또한 1.5배 증가했으며 과학적으로 공정을 최적화해 일관되게 높은 품질의 제품을 안정적으로 생산할 수 있게 됐다.
대웅제약은 이번 프로젝트와 관련해 "QbD는 글로벌 제약시장에서 대세로 굳어지고 있지만, 국내 전문인력이 부족해 늘 아쉬움이 있었는데, 때마침 정부 당국의 시의적절한 협조가 큰 도움이 됐다"고 평가했다.
업계 관계자는 "최근 몇몇 제약사가 자료조작 의혹, 심각한 품질 부적합 논란 등에 휩싸인 데다, 코로나19로 제약업계가 주목받는 가운데 글로벌 진출도 탄력을 받고 있어 정부의 QbD 도입 명분은 더욱 커진 상황"이라며 "각 제약사는 정부의 QbD 정책 변화에 대처할 수 있도록 지금부터라도 철저히 준비할 필요가 있다"고 말했다.






