
[헬스코리아뉴스 / 박민주] 알츠하이머의 원인으로 알려져 있는 아밀로이드 베타(Amyloid-β, Aβ) 올리고머를 나노입자 표면에 합성, 이를 분해하는 화합물이나 생체단백질을 빠르게 발굴할 수 있도록 돕는 새로운 플랫폼이 개발됐다.
고려대학교 윤대성 교수 연구팀이 광운대학교 이정훈 교수, 고려대학교 이규도 교수, 경희대학교 황교선 교수와 공동으로 연구해 나노입자 표면에 단백질 코로나(단백질들이 나노입자 표면에 응집해 이룬 응집체) 형태로 아밀로이드 베타 올리고머를 합성, 올리고머만 선택적으로 분해하는 화합물을 탐색(스크리닝)할 수 있는 플랫폼을 개발했다.
이번에 개발된 플랫폼을 이용하면 화합물을 탐색하는 데 걸리는 시간을 기존 수 일에서 하루 이내로 단축할 수 있으며 고가인 아밀로이드 베타를 기존 대비 50배 이하만 사용해도 탐색이 가능하다. 연구팀은 이번 성과로 알츠하이머 치료제 후보물질 발굴이 활발해질 것으로 기대하고 있다.
현재 알츠하이머병의 주요 원인물질은 아밀로이드 베타 올리고머가 거론되고 있으나, 순수한 올리고머는 합성과 정제가 어려운데다 표지할 수 있는 형광물질도 없어 이를 표적으로 하는 약물 후보물질을 대량으로 탐색하기가 어려웠다.
연구팀은 플라즈모닉 나노입자 표면에 단백질 코로나 형태로 순수한 아밀로이드 베타 올리고머 만을 코팅하는데 성공했다. 후보화합물에 의해 단백질 코로나가 분해될 시 나노입자 표면이 노출되고 서로 응집해 흡광도가 변화하면 용액이 적색으로 변하는 원리를 이용해 약물탐색 플랫폼을 개발했다.
①플라즈모닉 나노입자 : 국소 표면 플라즈몬 공명 현상을 띄는 금속나노입자이다.
②국소화 표면 플라즈모닉 현상 : 금속 나노입자와 빛이 반응하여 일어나는 광학적 특성. 나노입자의 크기 및 구조에 따라서 독특한 흡광특성을 나타낸다.
형광물질이나 추적을 위한 추가 처리 없이 용액의 색 변화로 올리고머를 선택적으로 분해하는 화합물이나 생체단백질을 선별할 수 있게 된 것이다.
연구팀은 실제 알츠하이머 완화에 도움이 된다고 알려진 저분자 화학물질 6종 및 생체 내 아밀로이드 베타를 제거하는 생체단백질 2종을 이용해 이 플랫폼을 검증했다.
이번 연구 결과는 국제학술지 '네이처 커뮤니케이션즈(Nature Communications)'에 27일 게재됐으며, 과학기술정보통신부와 한국연구재단이 추진하는 중견연구사업, 원천기술개발사업 및 4단계 BK21 사업 등의 지원으로 수행됐다.
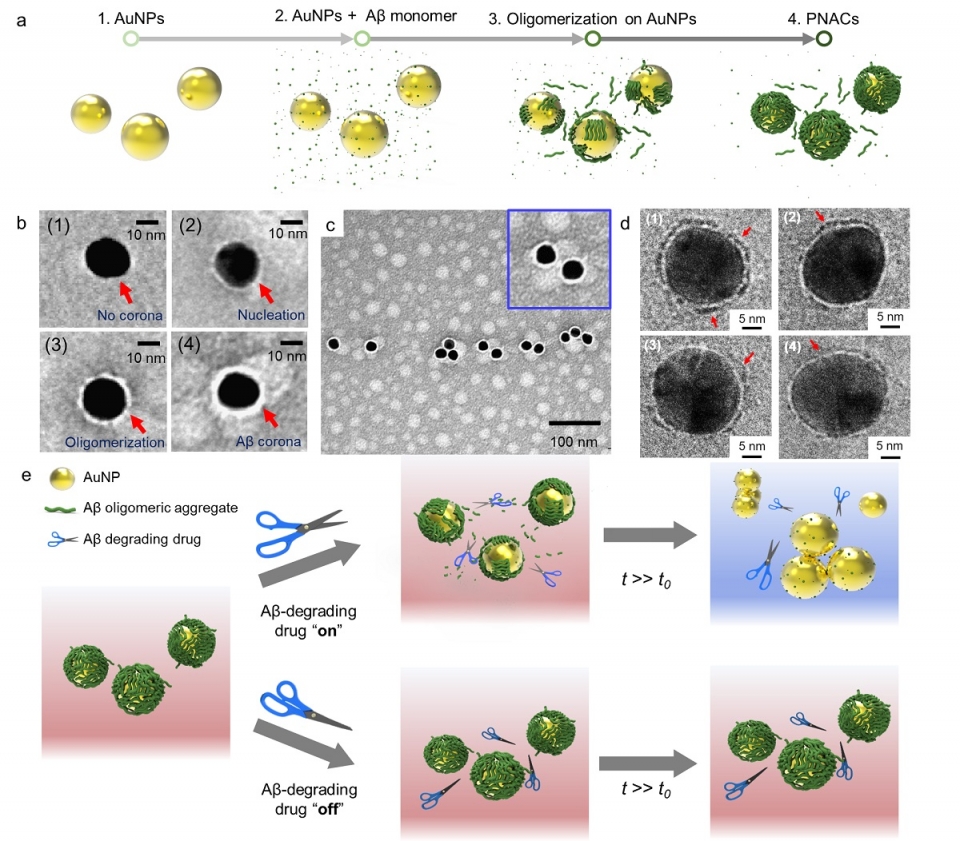
(a) PNAC의 복합체 형성 과정.
(b, c) 형성과정의 TEM 이미지.
(d) 약물 처리에 따른 아밀로이드 코로나의 분해 양상 Cryo-TEM 이미지.
(e) PNAC을 이용한 비색법 약물 스크리닝.
플라즈모닉 나노입자를 기반으로, 아밀로이드 베타 (Amyloid-β, Aβ)를 증착시켜 단백질 코로나 형태로 플라즈모닉 나노입자 아밀로이드 코로나 (PNAC)을 합성했다.
이 기술은 나노입자 응집에 의한 국소 플라즈몬 공명 (Localized surface plasmon resonance, LSPR) 현상을 기반으로 해 용액의 색 변화를 통해 (비색법) 약물의 효능을 정량적으로 평가하는 기술이다.
그림 및 그림설명 제공 : 고려대학교 윤대성/이동택
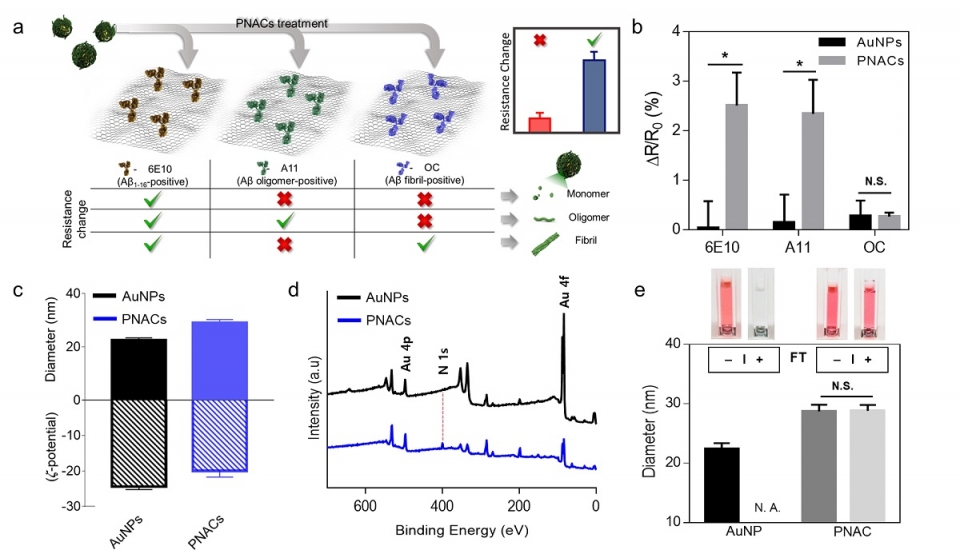
(a, b) 그래핀-항체 바이오센서를 이용한 아밀로이드 코로나 구성 검증.
(c) PNAC의 표면전하 및 크기 분석.
(d) XPS를 이용한 PNAC의 성분 분석.
(e) PNAC의 동결-건조 테스트 결과
PNAC 표면에 존재하는 아밀로이드 코로나의 형태적 특성을 파악하기 위해 그래핀-항체 바이오센서를 이용했다.
Aβ 특이적 6E10 항체, 올리고머 특이적 A11 항체 및 피브릴 특이적 항체 OC를 통해서 아밀로이드 코로나의 형태적 특성을 알츠하이머의 주 원인 물질로 알려진 Aβ 올리고머임을 검증했다.
또한 다양한 생화학적 검증 방식을 통해 균일한 아밀로이드 코로나가 PNAC 표면에 형성됨을 확인했다.
그림 및 그림설명 제공 : 고려대학교 윤대성/이동택

Aβ를 분해할 수 있는 단백질 효소로 알려진 Protease XIV와 Metrix metallopeptidase 9 (MMP-9)을 통해 Aβ 올리고머 분해 효능을 정량적으로 분석했다.
특히, MMP-9의 경우는 Aβ의 구성의 종류 (Aβ(1-42) 또는 Aβ (1-40)에 따라 분해 활성이 극명히 다름을 규명했으며, 효소 활성을 극저농도 (10 fg/ml) 수준에서 검출이 가능함을 확인했다.
그림 및 그림설명 제공 : 고려대학교 윤대성/이동택
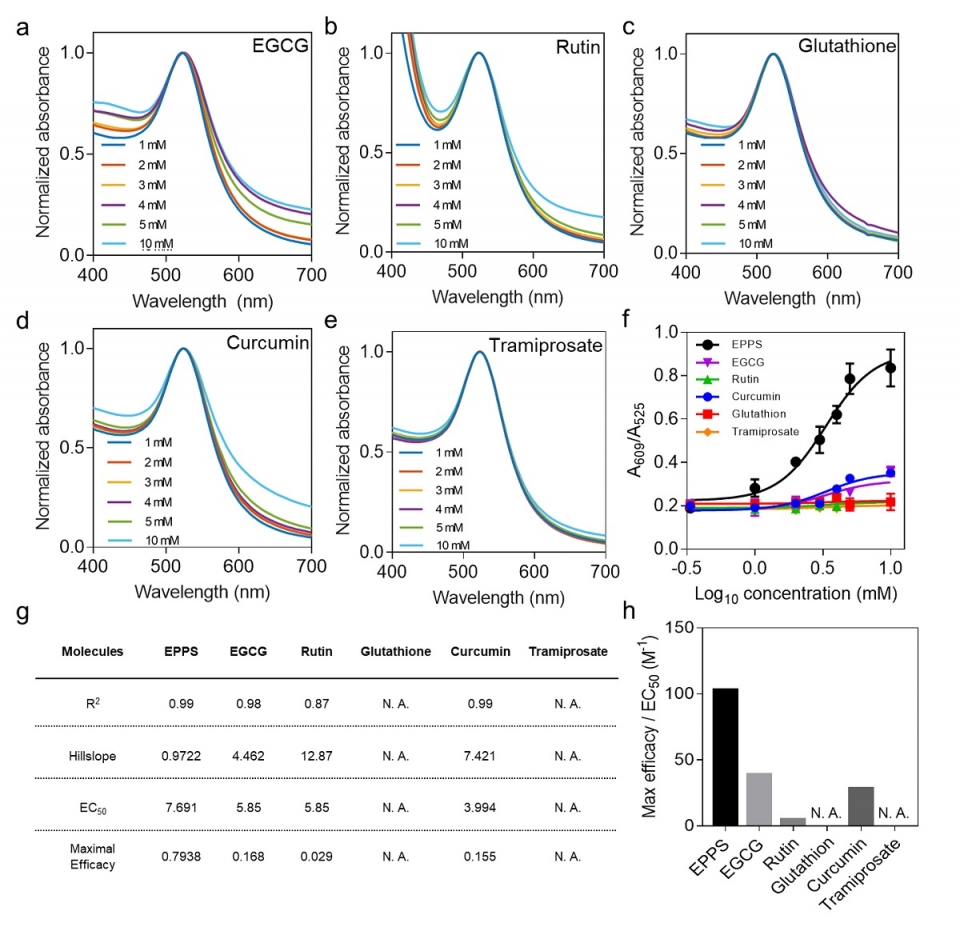
(a-e) EGCG, curcumin, glutathione, rutin 그리고 tramiprosate 처리에 따른 PNAC의 흡광도 변화
(f) 용량-반응 관계 (dose-response relationship)로 모델링한 각각의 약물의 분해효과 정량화
(g) 이에 따른 파라미터 (Hillslope, ECG50, Maximal Efficacy)
(h) Max efficacy/EC50으로 나타낸 각각의 약물의 아밀로이드 분해 효능
PNAC을 이용하여 알츠하이머 치료에 도움이 된다고 알려진 저분자 물질들의 Aβ 올리고머 분해효과를 정량적으로 분석했다.
분석결과들을 바탕으로 본 연구팀이 개발한 약물 스크리닝 플랫폼은 알츠하이머 주 원인물질로 알려진 Aβ 올리고머 제거할 수 있는 약물을 발굴하는데 활용할 수 있음을 검증했다.
그림 및 그림설명 제공 : 고려대학교 윤대성/이동택






