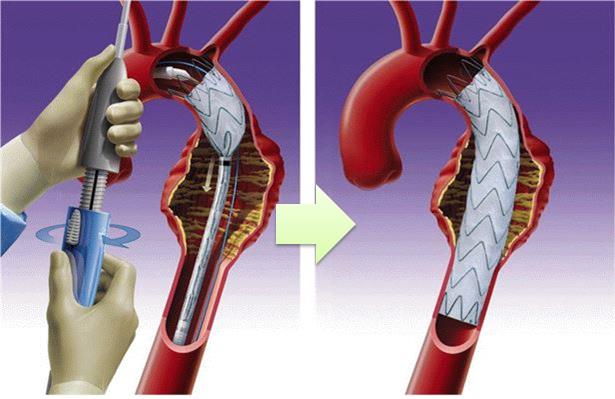
[헬스코리아뉴스 / 박민주] 혈관용스텐트에 대한 보건당국의 가이드라인이 마련됐다.
식품의약품안전처는 최근 다양한 혈관용스텐트의 개발이 활발해지자 ‘동맥류 등 혈관질환에 사용되는 혈관용 스텐트 허가·심사 가이드라인’을 제정했다.
혈관이 좁아지거나 막힌 곳에 삽입해 혈관내부를 확대하거나 동맥류, 혈관박리 등으로 혈관이 터지는 것을 막는 스텐트 등이 연이어 출시됨에 따라 이에 대한 분명한 가이드라인이 필요해서다.
이번 가이드라인은 혈관용 스텐트 제품 다양화에 맞춰 이에 대한 의료기기 허가·심사 방법 및 기준 등을 담고 있다. 구체적으로 ▲품목 분류 ▲허가 신청시 주요 부위의 치수 등 기재사항 ▲허가 심사시 안전성·유효성 입증자료 요건 ▲성능 평가 항목 및 시험방법 등이 제시돼 있다.
식약처는 “이번 가이드라인 출시에 이어 혈관용 스텐트의 품목을 세분화하는 품목 고시 개정도 준비 중”이라며 “이번 가이드라인 발간을 통해 관련 국내 제품이 안전성과 성능을 확보하고 신속한 제품개발과 수출경쟁력을 강화하는데 도움이 될 수 있기를 기대한다”고 밝혔다.
식약처는 “혁신적인 의료기기의 제품화를 적극 지원해 나가겠다”는 말도 덧붙였다.






