[헬스코리아뉴스 / 이순호] 식품의약품안전처가 코로나19 면역 진단시약 2개(항원 1개, 항체 1개) 제품을 정식 허가했다.
이번에 허가한 코로나19 면역 진단시약 중 ‘항원 진단시약’은 의료인 또는 검사전문가가 사용하는 제품으로 기존 유전자 진단 방식에 비해 정확도는 부족하지만 신속하게 결과를 확인할 수 있다고 식약처는 설명했다. 항원진단제품의 경우, 제출된 임상적 성능시험 결과에 따른 정확도는 민감도 90%, 특이도 96% 였다.
[코로나19 면역 진단시약 정식허가 제품 현황]
|
제조사 |
제품명 |
검사방식 |
허가일 |
|
에스디바이오센서㈜ |
STANDARD™ Q COVID-19 Ag Test |
면역(항원) |
11.11 |
|
에스디바이오센서㈜ |
STANDARD™ Q COVID-19 IgM/IgG Plus Test |
면역(항체) |
11.6 |
항체 진단시약
‘항체 진단시약’은 검체(혈액)로부터 항체를 분리하여 이와 결합한 물질을 통해 코로나19 바이러스(SARS-CoV-2)에 대한 항체 존재 여부를 확인하는 것이다.
이 제품은 15분 내외로 검사 시간이 짧으며, 과거 코로나19 바이러스 감염 이력을 확인할 수 있어 항체 생성 여부 확인 및 해외 입국 시 필요한 항체 검사결과 제출 등에 사용될 것으로 예상된다.
다만, 항체는 코로나19 바이러스에 대하여 면역반응이 나타났다는 것만 확인되며 바이러스 존재 여부는 알 수 없어 감염 진단 목적으로 사용하는 것은 적합하지 않다.
항체 진단시약의 허가는 짧은 시간에 손쉽게 감염 이력 확인이 가능하다는 데 의미가 있다.
항원 진단시약
‘항원 진단시약’은 검체(비인두 도말)로부터 코로나19 바이러스의 특정 성분을 검출하여 바이러스 감염 여부를 확인하는 방식으로, 30분 내에 검사가 가능하다.
이 제품은 증상이 있는 사람에게만 사용해야 하며, 유전자 진단시약 검사 결과와 임상증상 등을 고려하여 의사가 감염 여부를 최종 판단하도록 허가했다.
항원 진단시약의 허가는 대규모 확산 및 감염자 폭증 등의 감염 확산 상황에 따라 활용할 수 있는 검사방법에 대한 선택의 폭을 넓혔다는 데 의미가 있다.
이로써 식약처는 코로나19 유전자 진단시약 5개, 항원 진단시약 1개, 항체 진단시약 1개 등 총 5개 업체 7개 제품을 허가했다.
식약처는 현재 유전자 진단시약 14개, 항원 진단시약 4개, 항체 진단시약 11개 등 모두 29개 제품이 국내 허가를 신청하여 심사 중에 있다고 밝혔다.
[코로나19 진단시약 국내 허가 제품 현황]
|
제조사 |
제품명 |
허가일 |
검사방식 |
|
에스디바이오센서㈜ |
STANDARDTM M nCoV Real-Time Detection kit |
8.31. |
유전자 |
|
㈜바이오세움 |
Real-Q 2019-nCoV Detection Kit |
10.6. |
유전자 |
|
㈜시선바이오머티리얼스 |
U-TOPTM COVID-19 Detection Kit Plus |
10.8. |
유전자 |
|
㈜캔서롭 |
Q-Sens® COVID-19 Detection kit |
10.8. |
유전자 |
|
㈜코젠바이오텍 |
PowerChek™ SARS-CoV-2, Influenza A&B Multiplex Real-time PCR Kit |
11.3. |
유전자 (코로나19-독감 동시진단) |
|
에스디바이오센서㈜ |
STANDARD™ Q COVID-19 IgM/IgG Plus Test |
11.6 |
면역(항체) |
|
에스디바이오센서㈜ |
STANDARD™ Q COVID-19 Ag Test |
11.11 |
면역(항원) |
[코로나19 진단검사법 비교]
|
구분 |
유전자 검사 |
항원 검사 |
항체 검사 |
|
검사 목적 |
코로나19 바이러스 유전자 유무 확인
|
코로나19 바이러스 특정 단백질 유무 확인
|
코로나19 바이러스에 대한 항체 생성여부 확인 * 대규모 역학조사(항체가 조사) 및 혈장치료제 공여자 선정 등에 사용 |
|
검사 물질 |
바이러스 유전자 |
바이러스 특정 단백질 |
체내 생성 항체 |
|
사용 검체 |
비인두 또는 구인두 도말물 |
비인두 또는 구인두 도말물 |
혈액 |
|
검사 시간 |
약 3 ~ 6시간 |
약 15~30분 |
약 15분 |
|
장점 |
유전자를 증폭시켜 소량의 바이러스가 있어도 조기 진단할 수 있고, 정확도가 높아 확진용으로 사용 |
비인두 검체 등을 그대로 사용하여 유전자 검사 대비 검사시간이 짧고 비용 낮음 |
과거 감염이력 확인 가능하고, 검사시간이 짧고 비용 낮음
|
|
단점 |
과거 감염 이력 확인 불가, 검사시간 길고 비용 높음
|
검체를 증폭하지 않고 그대로 사용하여 바이러스가 미량인 경우 유전자 검사에 비해 정확도가 낮고, 검사결과에 영향을 줄 수 있어, 초기 무증상 환자를 확진하기에는 어려움 |
감염 초기 항체가 확인되지 않을 수 있고, 검사당시 검체 내 바이러스 유무 직접 확인하기 어려움
|
|
측정 원리 |
바이러스 유전자를 증폭하여 감염여부 확인 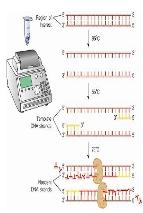
|
바이러스와 결합한 특정 물질을 검출하여 바이러스 감염여부 확인 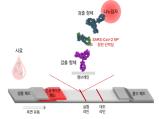
|
체내에 생성된 항체와 결합한 물질을 분석하여 항체 존재여부 확인 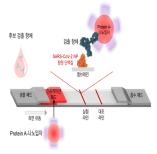
|
|
|
|
|
|
|
검사자 (사용자) |
의료인 또는 검사 전문가 |
의료인 또는 검사 전문가 |
의료인 또는 검사 전문가 |








