
[헬스코리아뉴스 / 박원진] 대장암 치료 후 재발의 원인이 되는 암 줄기세포 활성화의 분자적 기전이 밝혀졌다. 연세대학교 생명공학과 최강열 교수 연구팀이 대표적 암 억제인자인 p53이 역설적으로 암 줄기세포 활성화를 도와 암 재발을 유도하는 사실을 알아낸 것이다.
그동안 대장암 등을 위한 표준 화학치료요법으로 5-플루오로 우라실(5-FU) 기반 복합요법이 자리 잡은 지 오래되었지만, 치료 후 재발 시 나타나는 암 줄기세포 증가와 관련된 기전은 잘 알려지지 않았다.
연구팀은 먼저 대장암 환자의 암세포를 배양해 만든 오가노이드와 대장암 생쥐모델을 이용, 5-플루오로 우라실 치료 후 암 줄기세포가 활성화되는 것을 확인했다. (오가노이드(organoid)는 줄기세포를 3차원적으로 배양하여 특정 장기의 구조와 기능을 재현하기 위해 만든 장기 모사체를 말한다.)
미니장기처럼 암 환자 특이적인 조직 특징이나 생리 활성을 재현하는 암 오가노이드는 일종의 환자 아바타 모델로 임상 적용 가능성 확인에 주로 이용된다.
연구팀은 나아가 치료 후 암 재발과정에서 p53이 WNT 신호전달계를 자극, 암 줄기세포 활성화를 유도하는 사실도 밝혀냈다.
장(gut) 줄기세포를 배양, 장 오가노이드를 처음 제작·보고(2009년)한 한스 클레버 교수 연구팀(네덜란드 후브레흐 대학)과의 공동연구로 유전자 가위를 이용하여 p53이 소실된 장세포 유래 오가노이드를 확보, p53의 이같은 역할을 정교하게 검증했다.
※ p53은 대표적인 암 억제인자로 잘 알려져 있으며, DNA 손상이나 비정상적 성장신호 등이 있는지 세포의 상태를 모니터링하는 감시자 역할을 수행한다.
※ WNT 신호전달계는 암 발생과 진행에 중요한 신호전달계로, 대장암 환자의 90% 이상에서 APC라는 유전자의 돌연변이로 인해 이 신호전달계가 활성화 되어 있으며, 대장암 줄기세포 활성화에 중요한 것으로 알려져 있다.
이같은 결과는 5-플루오로 우라실의 약효 극대화와 재발 억제를 위해 WNT 신호억제제의 병용치료 필요성을 뒷받침한다.
실제 환자 암세포 유래 오가노이드와 대장암 세포를 이식한 동물 모델에서 WNT 신호전달계를 억제하는 화학물질을 함께 처리 하자, 5-플루오로 우라실에 의한 암 줄기세포 활성화가 저해되고, 단독처리 이후 발생하는 종양의 재성장이 억제됨을 검증, WNT 신호저해제가 효과적일 수 있음을 제시했다.
대표적 암 억제인자 p53의 암 줄기세포 활성화라는 상반된 역할을 밝혀내는 한편 그를 저지할 분자표적을 제시한 이번 연구성과는 교육부·한국연구재단이 추진하는 기본연구사업, 과학기술정보통신부· 한국연구재단이 추진하는 중견연구사업 등의 지원으로 수행되었다.
연결과는 국제학술지‘네이처 커뮤니케이션즈(Nature Communications)’에 10월 21일 게재됐다.
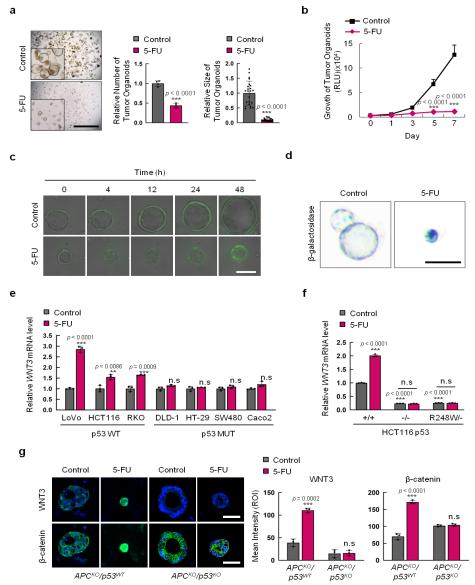
5-FU에 반응성이 있으며 Lgr5 관찰 가능한 대장암 모델 쥐 (ApcMin/+/Lgr5EGFP)의 암세포 유래 오가노이드에 5-FU 처리 시 Lgr5+ 암 줄기세포가 크게 증가되며, WNT 활성도 확인 가능한 유전자인 Axin2 관찰 가능한 대장암 모델 쥐 (ApcMin/+/Axin2LacZ) 암세포 유래 오가노이드를 이용해 5-FU 처리 시 WNT 신호전달계가 증가됨을 확인하였다. 또한, WNT 신호전달계의 활성화는 5-FU 처리에 의해 활성화되는 p53이 전사인자로 작용하여 증가시키는 WNT ligand의 발현을 통함을 사람 장 세포 유래의 오가노이드에 유전자 가위 Crispr/Cas9을 이용한 p53 knock-out을 통해 확인하였다.
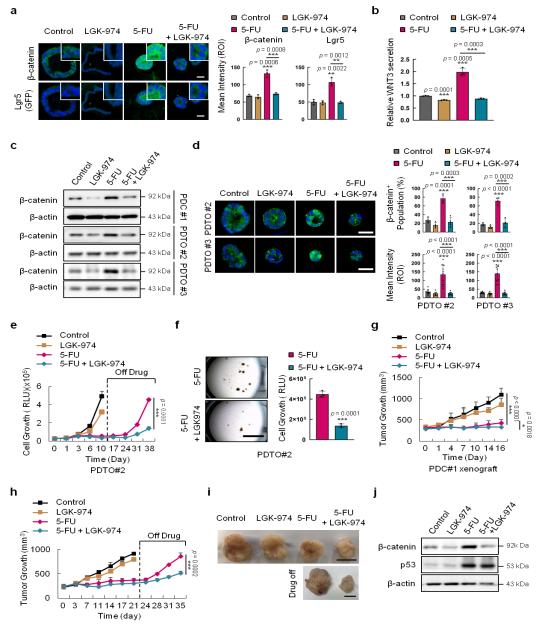
5-FU 처리 종료 후에 나타나는 대장 암세포의 재성장이 WNT 억제제와 5-FU 복합 처리 시에 크게 억제 되며, 이때 WNT 신호전달계 조절에 의한 암 줄기세포의 제어가 동반됨을 환자 암세포 유래 오가노이드 모델 및 이종 이식 쥐에서 확인하였다.
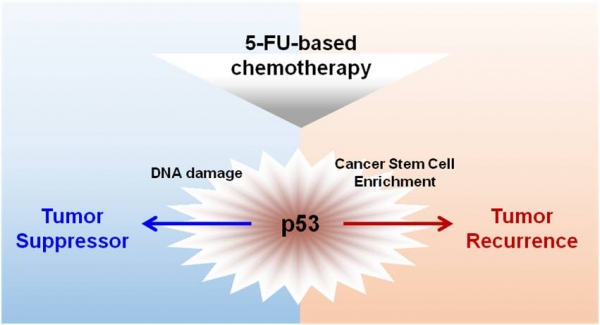
5-FU 치료 후 증가되는 p53은 DNA 손상에 의한 암세포 억제 기능과 동시에 암 줄기세포 증가를 통해 궁극적으로는 암 재발을 유도하는 양면성을 가지고 있다.
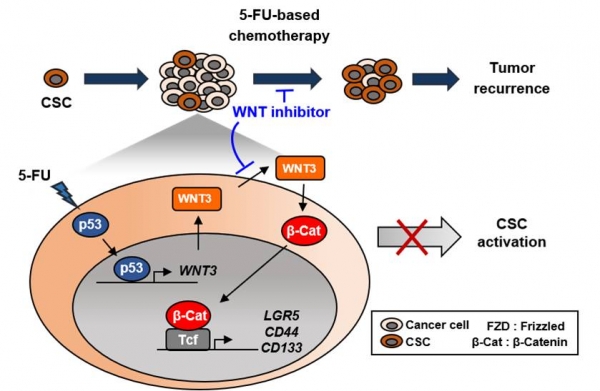
5-FU 치료 후 증가되는 p53은 WNT3의 전사인자로 작용하여 WNT 신호전달계 활성화를 유도하며, 활성화된 WNT 신호전달에 의해 암 줄기세포가 활성화 되어 재발을 유도한다. 따라서, 5-FU와 WNT 신호전달계 억제제를 병용처리시, 암 줄기세포 활성화로 인한 암의 재발을 억제하여 환자 사망률을 크게 증진 시킬 수 있다.
[연구자 인터뷰]
Q, 연구를 시작한 계기나 배경은 무엇인가.
“대장암은 장 내시경 등 조기진단과 화학 항암제의 발전으로 생존율이 증가되고는 있지만, 여전히 전 세계적으로 암 관련 사망률이 3번째로 높은 위험한 질병이다. 다양한 세포 독성 화학항암제(5-FU, Oxaliplatin, Irinotecan), 표적항암제(Cetuximab, Panitumumab)의 개발에도 불구하고, 이들의 제한적인 효과로 인해 임상에서는 주로 5-FU를 기반의 복합치료요법이 사용되고 있다. 하지만, 이 역시 50% 이상의 대장암 환자에서 초기에는 약효를 보이지만, 높은 재발률로 인해 환자의 5년 생존율은 크게 증가시키지 못하는 한계가 있어 5-FU기반 치료 후, 재발을 억제할 수 있는 작용 기작에 대한 연구를 시작하게 되었다.”
Q, 연구 전개 과정에 대해 소개해달라.
“5-FU 처리 시, 암세포 사멸이 일어남과 동시에 대장암 줄기세포 마커인 Lgr5+ 암세포가 증가됨을 통해 5-FU치료 후 발생하는 대장암 재발에 암 줄기세포의 관련성을 확인하였고, 5-FU 처리 시, WNT 신호전달계 활성화 이후에 암 줄기세포가 증가됨 확인하였다. 다양한 세포 및 대장암 모델에서의 p53 유전자 조작를 통해 5-FU 처리 시 활성화되는 p53이 WNT ligand의 전사 인자로 작용하여 WNT 신호전달계를 활성화시킴으로써 암 줄기세포를 증가시키는 주요한 인자로 역할을 함을 규명하였고, 그 내용을 Nature Communications에 게재하게 되었다.”
Q, 연구하면서 어려웠던 점이나 장애요소는 무엇이었나?
“임상 적용 가능한 5-FU의 암 줄기세포의 활성화 메커니즘 규명 및 작용기작의 재발과의 관련성을 확인하기 위해 환자 암세포 유래 오가노이드 생체자원은행을 구축하였고, 연구 초기 당시 전 세계적으로 환자 암세포 유래 오가노이드가 보편적이지 않다보니 배양시스템 구축에 관련하여 많은 시행착오를 겪으며 많은 시간과 연구비를 투자해야 했다. 또한 대표적인 암 억제인자인 p53의 암 재발관련 인자로서의 양면성을 처음으로 암에서 규명하다 보니 다양한 시도를 통해 정확한 검증이 필요했으며, 암 오가노이드를 최초로 구축한 세계적으로 저명한 네덜란드의 Hans Clevers 교수 연구팀과의 공동연구를 통해 유전자 가위인 Crispr/Cas9을 이용한 p53 knock-out 사람 대장 오가노이드를 확보하여 5-FU처리 시 p53을 통한 암 줄기세포 활성화 기전의 임상 적용성을 확인 했다.”
Q, 이번 연구 성과 무엇이 다른가.
“p53의 경우 대표적인 항암 유전자로, 5-FU 기반 복합치료의 항암효과에 주요한 역할을 함이 잘 알려져 있다. 하지만 이번 연구는 이러한 p53의 양면성을 보여주는 연구로, p53이 암세포의 세포 자연사 유도 뿐 아니라 동시에 WNT ligand 발현을 증가시켜 대표적인 발암 신호전달계인 WNT 신호 전달체계를 활성화시키고, 이에 따른 대장암 줄기세포의 증가는 5-FU 기반 복합치료 이후 문제가 되는 재발에 주요한 역할을 함을 규명하였다. 이 같은 결과는 암 억제에 핵심적인 역할을 수행하는 p53이라는 종양억제인자의 양면성을 규명한 중요성을 더한다 하겠다. 5-FU의 암 줄기세포 활성화 작용기작의 제어효과를 다양한 대장암 환자유래 암세포 모델에서 검증함으로써 그동안 해결되지 못하였던 5-FU 기반 복합치료 후 재발을 억제하는 새로운 치료 전략을 제시하였다고 할 수 있다.”
Q, 실용화된다면 어떻게 활용될 수 있나?
“현재 임상에서 이용되는 FOLFOX, FOLFIRI 같이 세포 독성이 강한 항암제들로만 구성된 5-FU 기반 복합치료에 WNT 신호전달체계 억제 표적치료를 포함한 새로운 조합의 가능성을 보여주어, 5-FU 기반 복합치료 후 빈번히 발생하는 암 재발로 인한 환자사망 문제점 해결 하는데 크게 기여 할 수 있을 것으로 기대된다.”
Q, 꼭 이루고 싶은 목표나 후속 연구계획이 있다면?
“이 연구결과를 기반으로 기존 항암제 치료 후 재발 및 전이 등을 제어하여 기존 항암제의 한계를 극복하고, 현재 나아가고 있는 정밀의학(Precision Medicine)에 바탕을 두고 실질적으로 환자의 예후를 증진시킬 수 있는 효과적인 치료법 개발의 발판이 되었으면 한다.”






