[헬스코리아뉴스 / 서정필] 자궁내막암(endometrial cancer)에 관련된 수십 개에 달하는 단백질 분자들의 유전적 변화 매커니즘이 미국 연구팀에 의해 밝혀졌다.
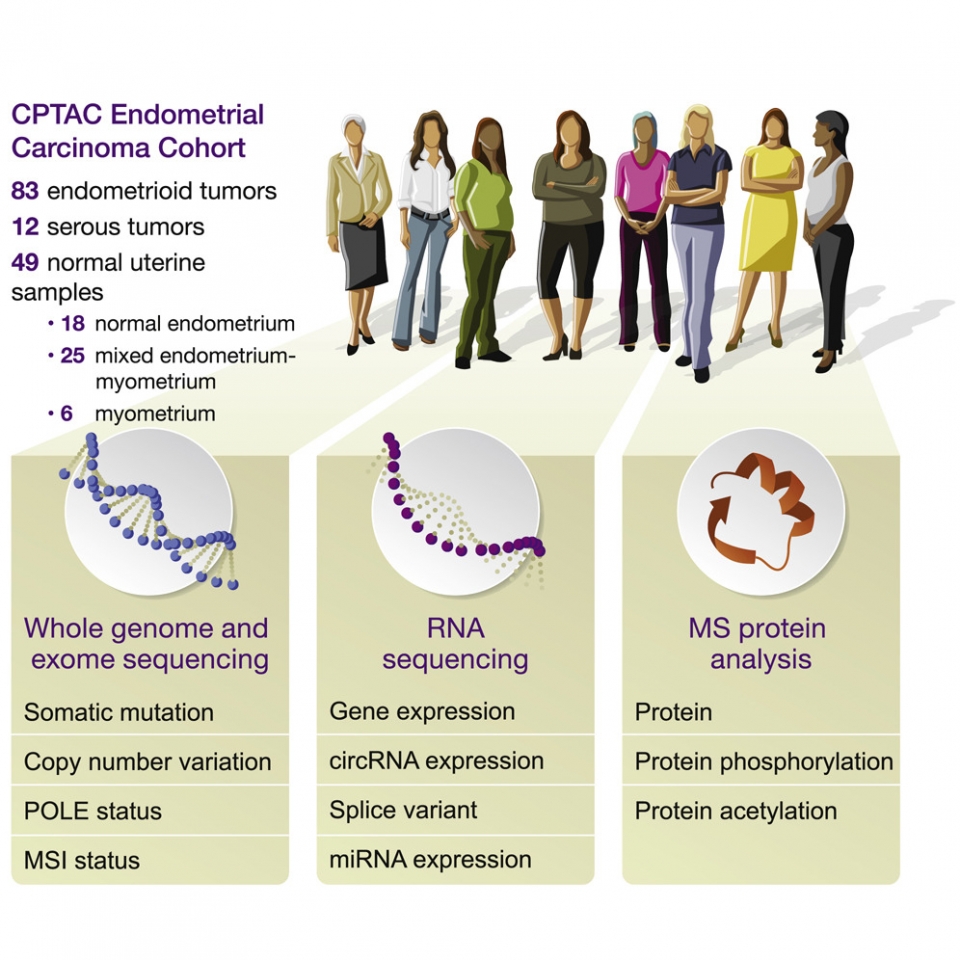
미국 워싱턴대와 뉴욕대 등 12개 기관 합동연구팀은 자궁내막 종양 95개와 49개의 정상 자궁 조직을 대조 분석해 이 같은 결과를 얻었다. 연구팀은 암종과 정상조직의 유전자, 단백질, 메신저 RNA, 원형 RNA, 마이크로 RNA 등의 빈도와 변형 및 위치를 모두 측정했다고 설명했다. 이번에 분석 대상이 된 분자의 작용은 모두 1200만 개에 달한다.
연구팀은 “이번 연구를 통해 자궁내막암을 치료하는 의료진들은 어떤 환자에게 좀 더 공격적인 치료가 필요한지 또 어떤 이유로 일부 환자에게는 일반적으로 치료가 효과적이지 않은지 판단할 근거를 갖게 됐다”고 밝혔다.
우선 이번 연구를 통해 자궁내막암에서의 그 작용 기전이 밝혀진 대표적 요소로는 베타-카테닌(beta-catenin)이 있다.
연구팀은 베타-카테닌 단백질이 자궁내막암 세포가 자라는 과정에서 어떻게 면역 체계의 탐지를 피하고 이를 성장하도록 자극하는지에 대한 중요한 역할을 하는지에 대한 구체적 작용 방식을 밝혔다.
연구팀은 또 환자마다 앓고 있는 암이 얼마나 공격적인지 판별하는 대표적 잣대로 ‘히스톤 아세틸화(Histone acethylation)’ 작용 정도를 소개했다.
‘히스톤(Histone)’이란 DNA를 구성하는 네 가지 염기인 아데닌·티민·구아닌·시토신을 엮어 감싸는 실패(絲牌, 실을 감는 나무패) 같은 역할을 하는 단백질인데, ‘히스톤 아세틸화’ 작용은 이 DNA 발현을 더 활발하게 하는 역할을 한다. 연구팀은 자궁내막암의 난소 전이 과정에서 ‘원형 RNA(circular RNAs)’의 역할도 밝혀냈다.
“이번 연구 과정에서 그동안 상대적으로 주목받지 못했던 원형 RNA가 세포 확산 임무를 수행하게 되면서 난소로의 전이 과정이 빨라진다”고 연구팀은 설명했다.
이번 연구에 수석저자로 참여한 데이빗 펜요(David Fenyö) 뉴욕대학교 유전학연구소 교수는 “이번 연구는 단백질 분석을 통해 특정 종양에서 가장 활동적인 단백질을 식별하고 환자마다 가장 효율적인 치료법을 설계할 수 있는 가능성을 높였다”고 말했다.
이번 연구 결과는 ‘자궁내막암에서의 단백질 특성 분석(Proteogenomic Characterization of Endometrial Carcinoma’이라는 제목으로 국제학술지 ‘셀(cell)’ 최근호에 실렸다.






