[헬스코리아뉴스 / 박정식] 암세포의 분석 정확도를 높이는 유전자 검사법이 국내 연구진의 의해 개발됐다.
11일 과학기술정보통신부에 따르면 연세대학교 의과대학 김상우 교수 연구팀은 환자의 암세포 시료를 분석할 때 외부요인을 줄여 분석의 정확도를 높이는 방법을 개발했다.
보통 환자의 치료과정에서 유전자검사나 약물반응검사 등을 위해 종양조직을 여러차례 분석해야 한다. 이에 한 번 채취한 종양세포를 자연적으로 보존하고 충분히 증식시켜 여러 검사의 시료로 쓸 수 있도록 하는 환자유래모델(PDMS, patient-derived models)이 활용된다.
다만 종양세포를 주로 생쥐(mouse)의 체내에서 증식시키거나, 생쥐의 세포와 함께 배양하기 때문에 쥐의 세포가 함께 분석돼 자칫 잘못된 결과가 나올 수 있다는 문제점이 있다. 이 같은 문제점이 꾸준히 제기되고 있지만 발생빈도나 예방방법에 대해서는 현재까지 알려진 바가 없다.
연구진은 환자유래모델에서 있을 수 있는 돌연변이 분석 오류를 찾아내고, 나아가 미연에 오류를 방지하는 방법을 개발했다.
우선 쥐와 사람에게서 나타나는 모든 유전자 서열 차이를 찾고 이를 ‘하마’(HAMA, human-genome aligned mouse allele) 라고 명명했다.
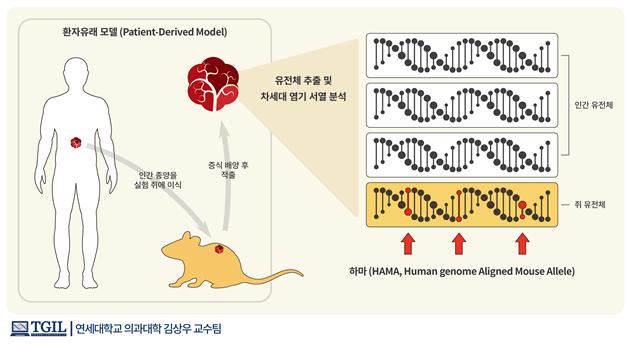
분석과정에서 이러한 ‘하마’가 나타난다면 질병 관련 유전 변이로 오인할 수 있는데, 생쥐의 유전체 정보로 인한 오류가능성을 한 번 더 확인하도록 안전장치를 제안한 것이다. 특히 잘 알려진 암 관련 돌연변이 데이터베이스의 정보 중 생쥐를 이용한 실험모델에서 비롯된 경우 유독 ‘하마’의 관찰빈도가 높게 나타난 것도 확인했다.
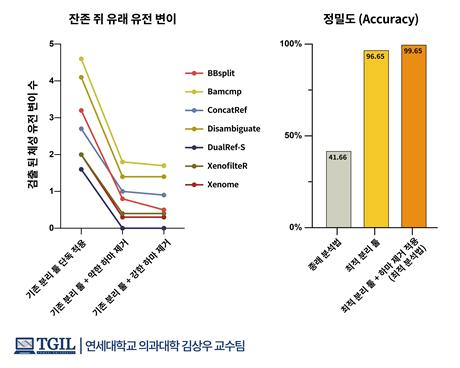
나아가 연구진은 유전체 검사 데이터를 통해 나오는 ‘하마’의 비율을 토대로 환자유래모델에 섞여 있는 쥐 세포의 비율까지 계산할 수 있는 방법을 제시했다. 또한 150가지가 넘는 가상의 오염 데이터를 기반으로 비교 분석을 수행해 최적의 오염 배제 방법을 밝혀냈다. 실제 이를 토대로 최적 유전자분석법을 적용한 결과 기존 분석 대비 정확성을 약 58% 가량 높일 수 있었다는 설명이다.
김상우 교수는 “본 연구는 체외에서 보존, 증식된 환자 암세포 시료(Specimen)의 유전체 분석과정에서 발생할 수 있는 오류를 바로잡은 것”이라며 “향후 더욱 정확한 정보에 기초해 환자를 치료할 수 있는 실마리가 될 것”이라고 말했다.
이번 연구는 과학기술정보통신부 개인기초연구(중견연구) 사업의 지원으로 수행됐다. 연구 성과는 유전체학 분야 국제학술지 ‘지놈 바이올로지’(Genome Biology) 11월11일자에 게재됐다.
아래는 연구진과의 미니 인터뷰.

|
◇ 연구를 시작한 계기나 배경은? 환자유래모델을 이용한 유전체 분석 진행시, 예상보다 훨씬 많은 양의 쥐 유전체가 포함돼 있음을 발견했고, 인간 유전체 분석에 큰 혼란을 주고 있음을 알게 됐다. 이를 계기로 쥐 유전 서열의 분리 및 제거에 대한 최적 분석 표준이 있어야겠다는 생각을 하게 됐다.
◇ 연구 전개 과정에 대한 소개 처음 연구를 시작할 당시에는 환자유래모델를 위한 분석 방법들이 조금씩 제시되기 시작할 때로, 분석법이 정립되지 않은 상태였기에 기존의 제시된 방법들을 바탕으로 최적 유전자 분석법을 만들고자 했다. 연구를 진행하면서 쥐 유래의 위양 변이를 인간의 변이와 구분할 수 있는 ‘하마’의 개념을 정의했고 이를 이용해 기존의 방법보다 정확도를 높일 수 있는 환자유래모델에 대한 최적 유전자 분석법을 제시할 수 있었다.
◇연구하면서 어려웠던 점이나 장애요소는 무엇인지? 쥐의 유전체와 암 환자의 유전체를 비교 분석시 외부 요인으로 인한 오차를 최소한으로 하기 위해 동일한 환경에서 제작된 유전체 데이터가 필요했다. 그러나 기존에 발표된 연구 데이터에서는 해당 조건에 맞는 데이터를 구할 수가 없어 직접 쥐의 조직을 채취하고 암환자 데이터 분석 시와 동일한 환경을 구축해 쥐의 유전체 데이터를 제작해 비교 분석 연구를 진행했다.
◇ 이번 성과, 무엇이 다른가? 차세대 염기서열 분석법(NGS)을 이용한 인간의 유전서열 연구과정에 쥐의 유전체가 섞이면 어떠한 영향을 초래하는지를 처음으로 제시했다. 더불어 쥐 유전 서열을 분리·제거하기 위한 방법들이 발표돼 있기는 하지만, 각각의 방법들이 얼마나 성공적인지, 그중 어떤 방법이 최적인지, 제거에 실패한 쥐의 유전 서열을 추가로 제거할 방법은 없는지에 대한 대답을 제시함으로써 차별성 있는 연구 성과를 거뒀다.
◇ 실용화된다면 어떻게 활용될 수 있나? 이번 연구 내용에서 관찰된 ‘하마‘와 정상 대립유전자 간의 비율을 이용하여 쥐 유전체의 오염도를 예측할 수 있는 공식을 도출해 냈다. 이를 근거로 쥐 유전체의 오염도를 간편하게 예측 할 수 있는 분석도구를 개발 중에 있으며, 실용화 된다면 환자 유전체 분석팀과 연구실에서 널리 쓰일 것이라고 예상한다.
◇ 꼭 이루고 싶은 목표나 후속 연구계획은? 이번 연구를 통해 정립한 ‘하마‘를 바탕으로 암 환자의 유전체 데이터에서 쥐의 유전체의 오염 비율을 환자 개인에 맞추어 정확히 계산할 수 있는 분석 도구를 개발하고자 한다. 또한 보다 정확한 유전체 분석을 위해 앞에서 언급한 쥐의 유전체 오염비율을 계산하는 도구를 응용하고, 쥐의 유전체를 환자의 유전체 데이터에서 제거하여 순수 인간 유전체 데이터를 얻을 수 있는 도구를 개발하여 환자유래모델을 이용한 개인 맞춤 치료에 도움이 되는 연구를 후속 연구로 진행하고자 한다.
◇ 기타 특별한 에피소드가 있었다면? 우리 연구팀은 직접 동물 실험을 수행하는 것이 아니라 생명정보학을 바탕으로 컴퓨터를 이용한 분석만을 수행하기에 실제 쥐 시료를 얻는 부분에서 어려움이 많았다. 주변 교수님들을 수소문해, 쥐를 희생(sacrifice) 하는 날을 알아내고 그 쥐에서 간을 얻을 수 있는지 여쭤보는 데에 시간이 걸렸다. 다행히 한 교수님께서 흔쾌히 이를 허락하셨고 시료를 얻어 연구를 시작할 수 있게 됐다. |






